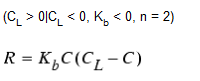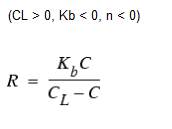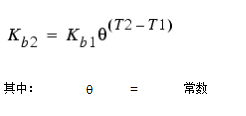流量体积反应
当某种物质在管道中向下移动或驻留在储罐中时,它会与水柱中的成分经历反应。反应速率通常可以描述为浓度的幂函数:
当存在针对物质的最终增长或损失的极限浓度时,速率表达式将变为:
不同反应速率表达式的一些示例如下:
简单 1 级衰减
许多物质(例如氯)的衰减可以建模为简单一级反应。
一级饱和度增长
此模型可应用于消毒副产品(例如三卤甲烷)的增长,其中副产品(氯)的最终构成受所存在的反应前体限制。
双成分二级衰减
此模型假定物质 A 以某个未知比率与物质 B 发生反应,以产生产品 P。A 的消失率与剩余 A 和 B 的产品成比例。CL 可以是正数,也可以是负数,具体取决于成分 A 或 B 是否过多。Clark 已于 1998 年成功将此模型应用于不符合简单一级模型的氯衰减数据。
米-门二氏衰减动力学
有一个特殊案例是,当指定负反应级数 n 时, HAMMER 将对衰减反应使用上面显示的米-门二氏速率方程。(对于增长反应,分母将变为 CL + C。)此速率方程通常用于描述酶催化反应和微生物生长。此方程会在低浓度下产生一级行为,并在较高浓度下产生零级行为。请注意,对于衰减反应,必须将 CL 设置为高于所存在的初始浓度。
Koechling 已于 1998 年应用了米-门二氏动力学来对许多种不同水质中的氯衰减进行建模,并发现了 Kb 和 CL 可能都与水的有机质含量及其紫外吸光度相关,如下所示:
零级增长
此特殊案例可用于对水龄进行建模,其中浓度(即水龄)会随时间单位的增加而增加。
在一个温度 (T1) 下观察到的体积反应速率常数与在另一个温度 (T2) 下观察到的体积反应速率常数之间的关系使用范特霍夫-阿伦尼乌斯方程来表示,其形式为:
在一项氯调查中,当 T1 为摄氏 20 度时,q 估计为 1.1(Koechling,1998 年)。